11月10日,復星醫藥強勢漲停,背后跟輝瑞宣布新冠疫苗90%有效的消息直接相關。
復星拼的不只是流量
11月9日晚間,輝瑞宣布其疫苗可預防90%的新冠病毒感染,遠超FDA(美國食品藥品監督管理局)要求的50%以上即可獲批上市標準,并計劃在11月的第三周向FDA提交緊急使用授權。根據目前的預測,輝瑞和BioNTech預計到2020年將生產多達5000萬劑疫苗,到2021年將生產多達13億劑疫苗。
據悉,復星醫藥除了持有輝瑞的這款新冠疫苗的相關權益外,復星醫藥還在今年3月獲得德國BioNTech授權,在中國大陸及港澳臺地區獨家開發、注冊、商業化基于其專有mRNA技術平臺研發的復星新冠疫苗(暫定名“復必泰”)。目前復星正與監管部門溝通,力爭盡快在國內啟動BNT162b2的橋接臨床試驗。
在11月6日,上海復星醫藥(集團)股份有限公司還發布了公告稱,控股子公司HengenixBiotech,Inc.收到美國FDA關于同意ACE2-Fc受體融合蛋白用于治療新型冠狀病毒肺炎進行臨床試驗的函。

該新藥為本集團自主研發的創新型治療用生物制品,為C末端帶有IgG1Fc的重組人血管緊張素轉換酶2融合蛋白,擬用于新型冠狀病毒肺炎的治療。
該新藥的作用機理為可以競爭性地與SARS-CoV-2病毒表面的Spike蛋白結合,從而抑制病毒與宿主細胞表面的血管緊張素轉換酶結合,最終達到抑制病毒感染的效果。該新藥的臨床前藥理學研究、藥代動力學研究及安全性評價證明,HLX71能夠顯著抑制SARS-CoV-2病毒感染,具有良好的安全性,可以用于開展后續的人體臨床試驗。
截至本公告日,全球范圍內尚無同類用于治療新型冠狀病毒肺炎的受體融合蛋白藥物獲得上市批準。
截至2020年9月,本集團現階段針對該新藥累計研發投入約為人民幣2,847萬元(未經審計)。
各國疫苗研發進展如何
目前在研發中的新冠疫苗按技術路線可分為病毒載體疫苗、mRNA疫苗、蛋白重組疫苗、減活/滅活疫苗和DNA疫苗五大類。據《紐約時報》數據,全球范圍內共有69個疫苗計劃正在進行中。
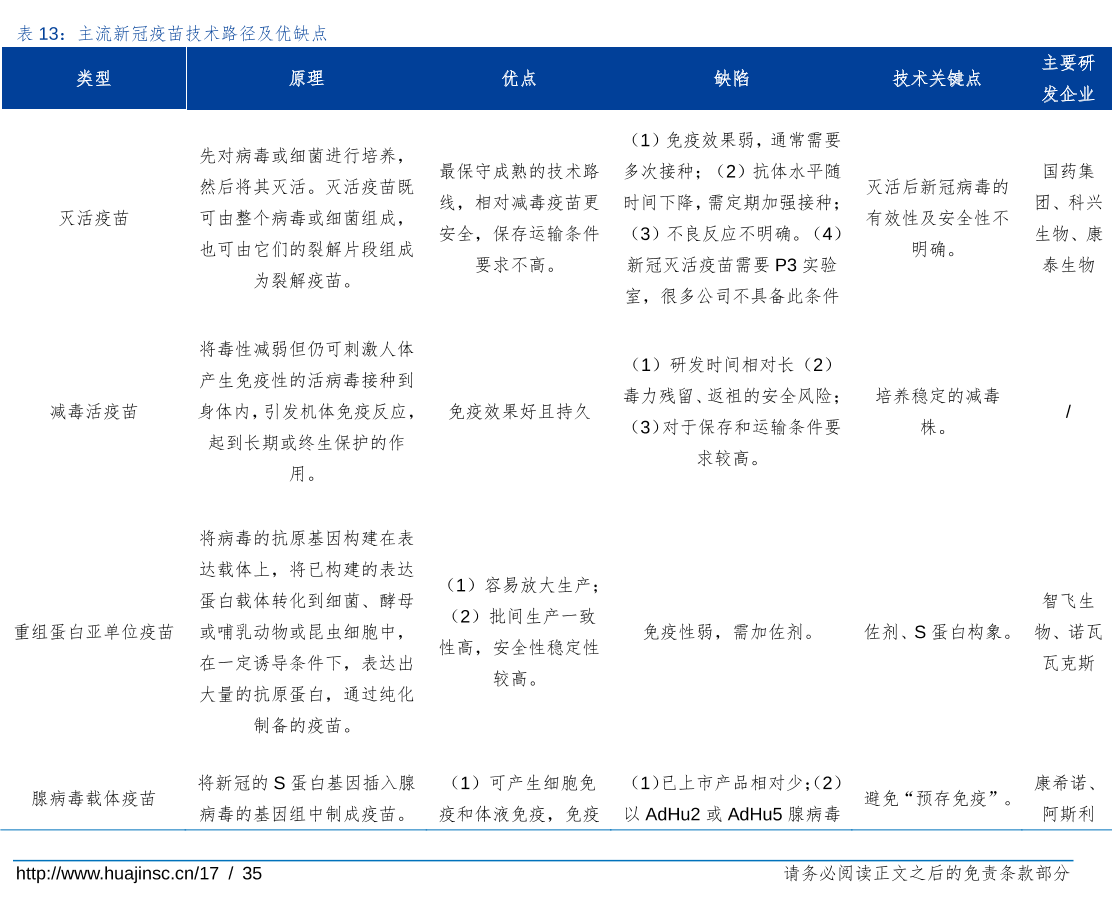
其中有11支疫苗已經進入了III期臨床試驗,其中包括90%有效的瑞輝mRNA疫苗,其余10支疫苗中有4支來自美國,2支來自中國,2支來自英國,剩余3支分別來自俄羅斯、印度和澳大利亞。
另外,在全球范圍內已經有6支中國和俄羅斯的疫苗獲得了批準,可以在沒有獲得III期臨床試驗結果前,在有限范圍內接種。
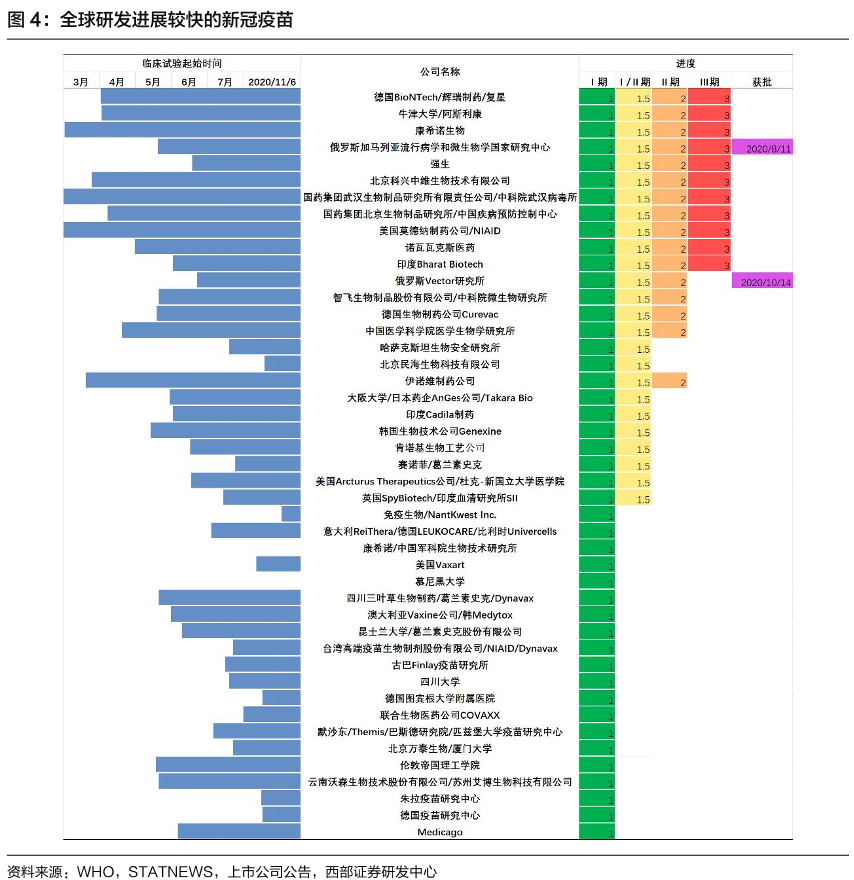
其中,由陳薇院士團隊和康希諾合作研發的病毒載體疫苗以及由北京科興生物制品有限公司研發的2支疫苗正在中國境內小范圍接種,而分別由國藥集團武漢生物制品研究所和北京生物制品研究所研發的2支疫苗正在阿聯酋小范圍接種。由俄羅斯研發的2支疫苗早已開始在俄羅斯進行小范圍接種。
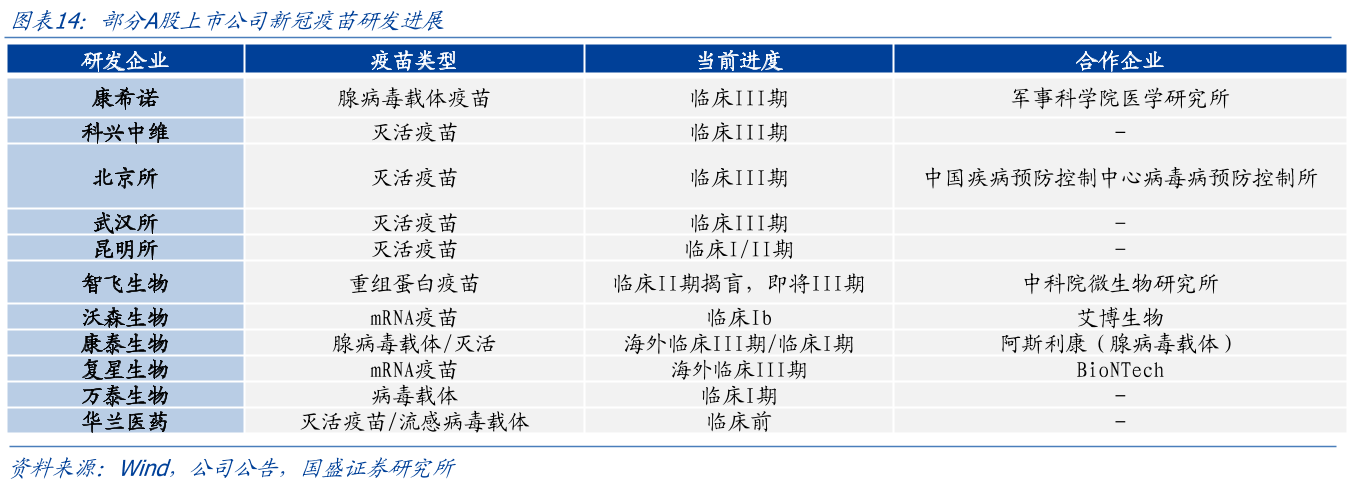
疫苗從研發到測試和生產,原本需要5到10年甚至更長時間,其中III期臨床試驗往往就需要進行數年。但由于新冠病毒的大流行與全球疫情的緊要,所有國家都將研發模式調整為了階段重疊式,按目前的進度,預計在明年年初就將有疫苗獲批投產。
千億市場機會逐步開啟
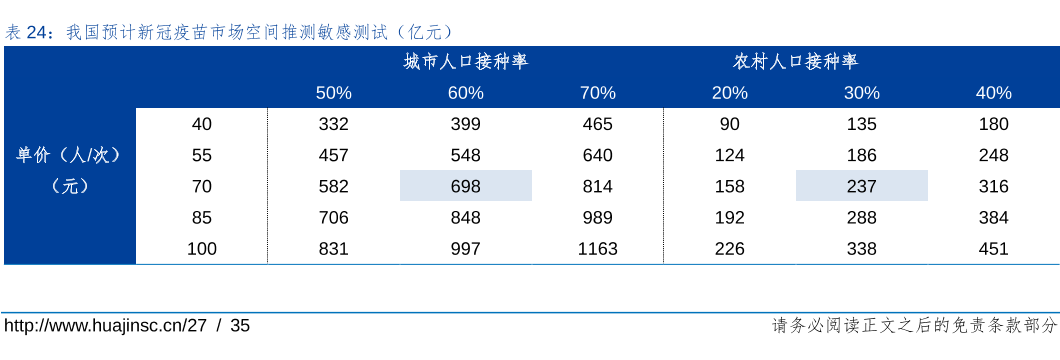
東興證券在10月份的一份研報中指出,國產疫苗啟動特殊審批上市程序后,國產滅活苗已開始針對特殊人群接種,參考浙江省疾控價格,每人份價格為400-800元。考慮前期免疫接種人群為自愿自費接種,定價體現企業自主選擇。同時,墨西哥和馬來西亞也公布疫苗采購的計劃,推算每人份均價在100-150元人民幣左右,而且墨西哥已經向康希諾采購3500萬劑,綜合國內外定價機制,預計新冠疫苗價格將超過100元/人份,對研發成功的企業,利潤空間足夠。國內+國外市場合計,新冠疫苗將成為千億級別的大品種。
中信證券表示,受益于國內疫情的快速控制,餐飲、酒店、景區的復蘇節奏本身已略超預期,而隨著新冠疫苗研發取得突破有望進一步加快行業修復,博彩、出境游等長距離出行板塊復蘇預期增強。但同時疫苗完全大面積接種仍需時日,期間局部地區疫情反復仍存影響,加之居民信心完全恢復也存在周期,疫苗的加快推出對行業景氣的影響并不會即刻顯效,只是有助于縮短總體恢復周期。
安信證券認為,航空受疫情影響最嚴重的時期已經過去,疫苗有望推動客流加速恢復,并提振市場風險偏好,看好順周期航空板塊輪漲,重點推薦低成本航空春秋航空;具備高品質航線的中國國航(國際線占比高,未來受益國際線復蘇);國內線占比高、業績彈性大的南方航空;區位優勢明顯的東方航空;關注支線航空華夏航空。
最后,借用一段網絡段子收尾。不管結果如何,投資者還是要有自己的理性判斷,對自己的投資負責。
“一般研究員:疫苗出爐,利好航空酒店餐飲;
優秀研究員:疫苗出爐,需求回升,通脹升溫利好大宗;
卓越研究員:疫苗出爐,需求回升,收入回升,通脹升溫,白酒漲價,利好白酒。”

